1 型糖尿病(T1D)是一类由多种免疫细胞参与的针对胰岛 β 细胞的自身免疫性疾病。目前,T1D 的主要治疗方式依然是胰岛素注射,虽能有效控制患者血糖平稳,却无法阻止胰岛功能进行性衰竭。针对 T1D 发病病因的免疫治疗目前仍在不断探索,但均未取得理想的效果。因此,探索 T1D 的免疫治疗方式具有重要的意义。
近期杨涛教授团队研究发现 Tfr 细胞的降低可能与 T1D 的发病机制有关,且 Tfr 细胞对治疗 T1D 具有潜在价值,其机制可能与增强保护性免疫,抑制自身免疫性糖尿病有关。该成果发表在 The Journal of Clinical Endocrinology & Metabolism 杂志上。
研究介绍
滤泡调节性 T 细胞 (Tfr) 是一类特殊的调节性 T 细胞亚群,其不仅能特异性地通过抑制 Tfh 细胞和 B 细胞以控制 GC 反应,同时还可以抑制 T 细胞的增殖活化。杨涛教授团队通过观察 Tfr 细胞在 1 型糖尿病中的表达水平,旨在探讨其是否参与 T1D 的发病机制。
研究招募了 T1D 患者与 2 型糖尿病 (T2D) 患者、T1D 患者的一级亲属 (T1D-FRs) 和健康对照进行研究,评估了外周血循环中两种经典 Tfr 细胞的比例和功能变化。同时杨涛教授团队还研究了 Tfr 细胞对 NOD 小鼠自身免疫糖尿病发展的影响,并通过过继转移模型来研究其治疗 T1D 的可能性。
研究结果
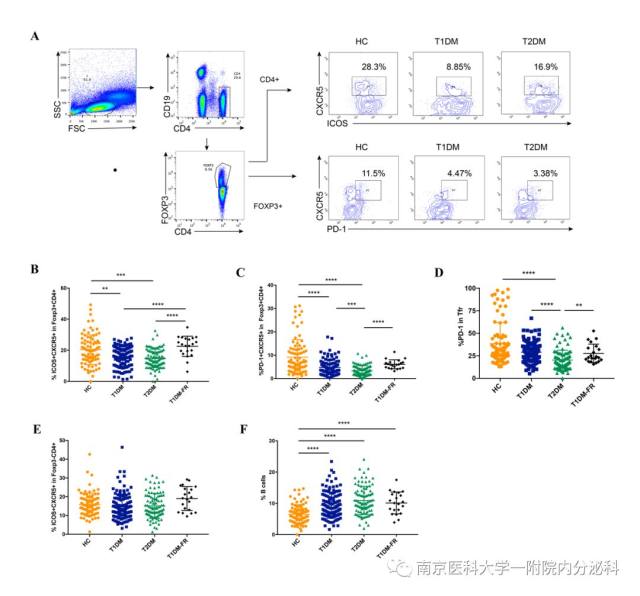
Tfr 细胞在不同人群中的差异
研究发现糖尿病患者的 Tfr 细胞较健康对照均明显减少。与 T1D 患者相比,T2D 患者 CXCR5+PD-1+ Tfr 细胞的比例更低。在对 T1D 患者的一级亲属研究发现:其 Tfr 细胞比例较健康对照无明显差异,而 CXCR5+ICOS+ Tfr 细胞比例较糖尿病患者明显增高。研究团队还进一步证明 Tfr 细胞与 T1D 患者胰岛功能呈显著正相关,与 GAD 胰岛自身抗体的滴度呈明显负相关。与糖化血红蛋白(HAb1c)及胰岛素使用未见明显相关性。此外,T1D 患者 Tfr 细胞对 T 细胞及 B 细胞功能的抑制能力要明显低于健康对照组的 Tfr 细胞。
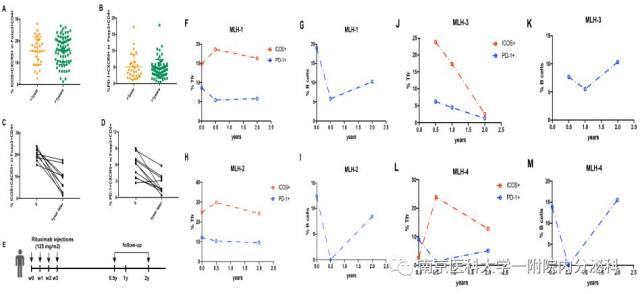
T1D 患者循环 Tfr 细胞的比例随病程和治疗的变化
在对 10 名患者进行为期 1 年的随访时发现,T1D 患者的 CXCR5+ICOS+ Tfr 细胞和 CXCR5+PD-1+ Tfr 细胞比例均有显著性的下降 (p = 0.0003, p = 0.0007)。说明随着 T1D 的进展,Tfr 细胞逐渐降低。研究者还观察了 4 例接受利妥昔单抗治疗的 T1D 患者的 Tfr 细胞比例。利妥昔单抗治疗后,3 例患者 CXCR5+PD-1+ Tfr 细胞频率降低,CXCR5+ICOS+ Tfr 细胞频率升高。这提示 PD-1 与 Tfr 细胞功能相关。该结果与之前动物研究结果是一致的。
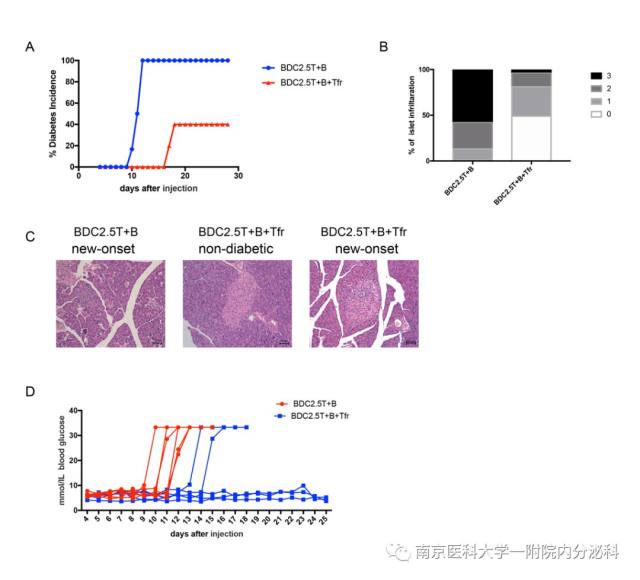
过继转移 Tfr 细胞可预防 NOD/SCID
小鼠的自身免疫糖尿病
杨涛教授团队还发现 Tfr 细胞与 NOD 小鼠自身免疫糖尿病的发生有关。为了进一步阐明 Tfr 细胞在对 T1D 的保护作用,研究者将 BDC 2.5 T 细胞和 B 细胞经尾静脉注射入 NOD-SCID 中构造了自身免疫糖尿病模型。干预组在注射入 BDC 2.5 T、B 细胞的同时注射入 Tfr 细胞。研究发现,与对照组相比,干预组糖尿病发病率显著降低: 从 100% 降至 33%。在 NOD-SCID 发病后监测血糖至造模 30 天后,摘取小鼠胰腺进行 HE 染色显示,Tfr 干预后的小鼠表现出较轻的胰岛炎,胰岛炎评分明显改善。
研究意义
研究表明,Tfr 细胞参与了 T1D 的发生和进展,为 T1D 的发病机制提供了新的方向。与此同时,Tfr 的免疫治疗可能为预防和治疗 T1D 提供新的靶点。
参考文献
Xu X, Shen M, Zhao R, et al.J Clin Endocrinol Metab. 2019 May 16. pii: jc.2019-00093. doi: 10.1210/jc.2019-00093
