随着对胰岛素抵抗(IR)的深入研究,现已认识到 IR 与炎症、内质网应激、线粒体功能障碍、细胞外基质有关;且涉及全身组织器官,更是多种疾病发病的「共同土壤」。结合刚结束不久的 2017 欧洲糖尿病研究协会(ESAD)年会 IR 的专题内容,我们再来认识一下多种疾病的罪魁祸首——IR 所带来的危害以及临床的应对启示。
2017 EASD 年会上,来自 Koutsovasilis 教授的新证据中 1,247 例合并非酒精性脂肪性肝病(NAFLD)的 2 型糖尿病(T2DM)患者,在二甲双胍治疗基础上,分别接受达格列净(n = 89)、西格列汀(n = 91)或吡格列酮(n = 67)治疗,平均随访 52 周。结果显示,达格列净及吡格列酮组患者,APRI 平均值(评估肝脏炎症和纤维化的替代指标)、天门冬氨酸氨基转移酶(AST)水平显著下降,而西格列汀组则无明显变化。对于肝脏炎症和纤维化改善程度而言,从数值上看,吡格列酮效果最佳。
那么吡格列酮为何表现如此优秀?与 IR 的改善是否存在关联?IR 是否还与其他疾病相关?下面让我们一探究竟。
IR 可导致非酒精性脂肪性肝病
NAFLD 是一种与 IR 和遗传易感密切相关的、肝脏脂肪过度堆积的代谢应激性肝脏损伤,与血脂代谢紊乱、中心性肥胖、T2DM 及代谢综合征密切相关。其发病机制尚不清楚,目前比较流行的是「二次打击」学说(如图 12),第一次打击即为 IR、游离脂肪酸代谢失调导致的肝脂肪变性,这与许多肝细胞适应性及信号通路的改变相关,为二次打击提供了肝细胞易感性。之后氧化代谢产物蓄积,引发氧化应激及炎症反应为第二次打击,使肝细胞发生炎症、坏死,诱发纤维化过程,最后使少数患者发生肝纤维化或肝硬化。
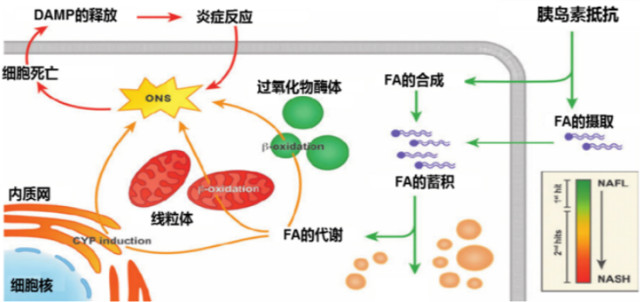
图 1. IR 导致 NAFLD 的机制
IR 亦可增加糖尿病心血管疾病发生风险
IR 是 T2DM 的主要发病机制,同时,IR 与心血管疾病(CVD)的发生亦相关。研究发现,1/3 处于 IR 状态的人群具有 CVD 患病风险,且该风险是无 IR 者的 1.67 倍;IR 程度越严重,冠心病风险越高(趋势 P<0.05),而根据 IR 程度分层后发现 IR 最严重者,CVD 风险较胰岛素敏感者增加 1.52 倍 3;相比空腹血糖和空腹胰岛素水平,IR 导致的心血管疾病发生风险更高 4。
IR 增加 CVD 患病风险的可能机制包括,IR 导致糖代谢异常、脂代谢异常、一氧化氮生成减少、诱发高血压,及降低纤溶活性等。具体的分子机制如图 2 所示 5:
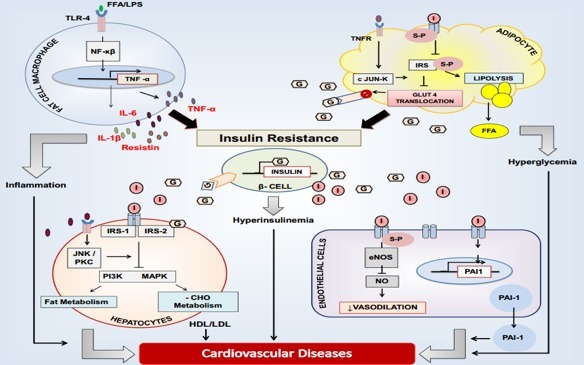
图 2:胰岛素抵抗导致心血管疾病的分子机制
IR 与 T2DM、NAFLD、CVD 之间相互影响
IR 可导致血糖、血压、血脂代谢异常,通过一系列作用影响 T2DM、CVD、NAFLD 发生发展,后三者又可互相影响 6(如图 3)。因此,改善 IR 对降低心血管事件风险、改善脂肪肝以及控制血糖意义非凡。
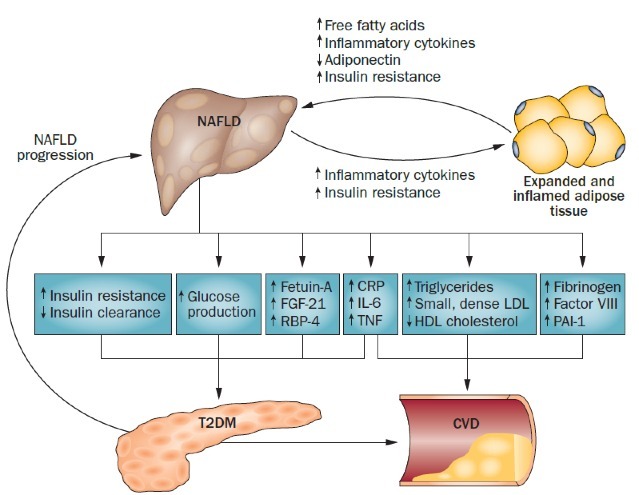
图 3. T2DM、NAFLD 与 CVD 三者之间的关系
从 IR 入手,让患者全面获益
综上所述,要使糖尿病患者全面获益,除生活方式干预外,还必须从根源 IR 入手。事实上,经典胰岛素增敏剂——吡格列酮,通过激活靶组织中的 PPARγ,调控与糖代谢、脂质代谢有关的靶基因,促进脂肪、骨骼肌对葡萄糖的摄取,减少肝脏葡萄糖的分解,从而改善 IR;此外,吡格列酮还可激活在代谢旺盛的组织上(肝脏、心脏等)表达极为丰富的 PPARα,使体内脂肪酸氧化/甘油酯化平衡趋向于分解代谢途径,降低心脏及肝脏脂肪酸的氧化水平,从而减少脂质积累,发挥心肝保护作用 7。
1) 吡格列酮调节脂代谢,改善脂肪分布,治疗 NAFLD
一项早期双盲、随机、多中心研究中,543 例患有冠脉疾病的 T2DM 患者随机接受格列美脲(1-4 mg)或吡格列酮(15-45 mg)治疗 18 个月,结果显示,吡格列酮显著增加 HDL-C,并降低甘油三脂水平 8。另一项研究显示,吡格列酮治疗 16 周后,患者皮下脂肪和内脏脂肪分布发生明显变化 9。
另一项研究比较了低剂量吡格列酮 30 mg/d、维生素 E 800 IU/天或安慰剂治疗非酒精性脂肪性肝炎(NASH)患者(n = 247)的疗效 10。结果显示,吡格列酮改善所有患者的组织学特征(除纤维化),缓解了脂肪性肝炎。患者使用吡格列酮治疗 96 周后,丙氨酸氨基转移酶水平、AST 水平均显著下降(P<0.001),且脂肪变性和小叶炎症显著改善(P<0.001)。
2) 吡格列酮延缓动脉粥样硬化,可能具有心血管获益
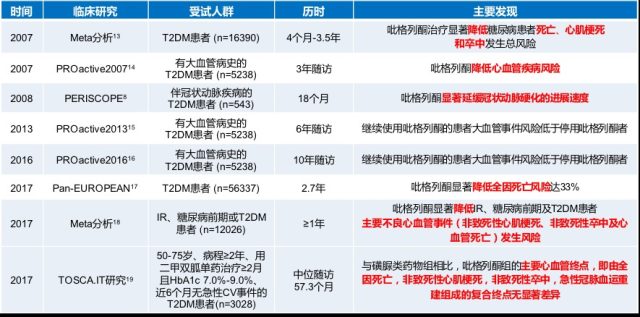
有研究显示,吡格列酮还可延缓颈总动脉内膜-中层厚度(CIMT)的增加,延缓动脉粥样硬化进展 8,11,同时改善脂代谢 11。大型对照研究,荟萃分析证实了吡格列酮具有心血管获益 13-19(表 1)。最新的第一个进行头对头来评估在二甲双胍治疗基础上加用吡格列酮或磺脲类药物对 2 型糖尿病患者心血管事件的长期影响的 TOSCA.IT 研究显示,吡格列酮与磺脲类药物的主要复合终点(全因死亡率、非致死性心梗、非致死性卒中和紧急血运重建)无显著差异。
表 1. 吡格列酮心血管获益的相关研究
小结
胰岛素抵抗与 T2DM、NAFLD 及 CVD 密切相关,改善 IR 对降低糖尿病患者心血管疾病,NAFLD 有重要意义。噻唑烷二酮类(TZDs)通过激活 PPARγ通路,改善 IR,同时又可激活 PPARα,发挥肝脏保护和心血管保护作用。从作用机理及临床研究来看,TZDs 药物可能对打破 2 型糖尿病患者「心糖肝」之间的相互作用产生积极影响。
参考文献
1. 2017 EASD, OP #12, A. Koutsovasilis, Effectiveness of dapagliflozin in nonalcoholic fatty liver disease in type 2 diabetes patients compared to sitagliptin and pioglitazone
2. https://www.researchgate.net/figure/259112226_fig2_FIG-2-Pathogenesis-of-NAFLD-Hepatic-insulin-resistance-increases-the-uptake-as-well-as
3. 邹大进. 诊断学理论与实践.2009.3(8):252-5。
4. Gast KB,et al. PLoS One. 2012;7(12):e52036.
5. Patel TP,et al.Heart Fail Rev. 2016 Jan;21(1):11-23
6. Anstee, Q. M. et al. Nat. Rev. Gastroenterol. Hepatol.19 March 2013.
7. Ye JM, et al. Diabetes. 2001 Feb;50(2):411-7.
8. Nissen SE,et al.JAMA. 2008;299(13):1561-73.
9. http://www.medscape.org/viewarticle/545748_2
10. Sanyal AJ, Chalasani N, Kowdley KV, et al. N Engl J Med 2010; 362: 1675–1685.
11. Mazzone T, et al. JAMA. 2006;296:2572-2581.
12. Choi SS, et al. BMB Rep. 2014 Nov;47(11):599-608.
13. Lincoff AM, et al. JAMA. 2007, 298(10):1180-1188.
14. Erdmann E, et al. Vasc Health Risk Manag 2007,3(4):355-370.
15. Erdmann E, et al. Diabetes Obes Metab 2014,16(1):63-74.
16. Erdmann E, et al. Diabetes Obes Metab 2016,18(3):266-273.
17. BMJ Open Diab Res Care 2017;5:e000364.
18. Liao HW, et al. BMJ Open. 2017, 7(1):e013927.
19. https://www.easd.org/virtualmeeting/home.html#!resourcegroups/query = TOSCA.IT
审批编号:CN/ACT/1709/0055d
