葡萄牙当地时间 9 月 12 日上午 8 点半,第 53 届欧洲糖尿病学会年会(EASD2017)在里斯本拉开帷幕。会议首日,三大重磅奖项颁出,糖感神经元、低血糖并发症、β细胞 DNA「开关」,成了获奖关键词。
智汇君带您速览首日精彩内容。
「数」说本届 EASD 年会

图 1 本届 EASD 主席 Juleen R Zierath 教授在开幕式上致辞
● 这是 1965 年 EASD 首届年会开办之后的第 53 届年会;
● 来自 130 多个国家的 15000 余名参会者,1200 多位学者将发言交流;
● 大会收到 2147 份论文摘要,其中 1266 份入选;
● 大会设 50 个主题专场,48 个口头报告专场,6 个 Poster 展示时间;
● 大会设 5 场颁奖演讲,今年新增 2 个特别环节——「EASD Young Academy」和「Rising Star Symposium」。
Claude Bernard 奖——「潜伏」在大脑中的糖感神经元可能是糖尿病发病「始作俑者」
Claude Bernard 奖是 EASD 的最高奖项,主要授予为糖尿病和相关代谢疾病领域的发展作出创新贡献的学者。
今年的 Claude Bernard 奖授予了来自瑞士的 Bernard Thorens 教授。
Bernard Thorens 教授来自洛桑大学整合基因组学中心,他毕业于日内瓦大学生物化学专业,获得生物免疫学博士学位之后,于美国剑桥怀海德生物医学研究所开展博士后工作,随后任教于洛桑大学。

图 2 Bernard Thorens 教授获奖现场
Bernard Thorens 教授的演讲题目为《以血糖为中心的糖尿病发病机制:从胰岛生物学到整合生理学及精准医学》。
Thorens 教授对 2 型糖尿病发病机制进行了探讨。传统的观点认为糖尿病是由胰岛素分泌和胰岛素作用之间的不平衡引起的,为了解释这种失调的原因,Thorens 教授做了一个假设并进行验证——体内血糖平衡的失调是由于体内血糖感受能力缺陷而造成的,需要特别关注大脑中糖感神经元在整体控制体内血糖机制中的作用。
在随后的研究中,Thorens 教授使用了各种动物模型、生理学和行为学研究方式。
结果证明在糖尿病前期,大脑中的「糖感神经元」控制了人体重要的生理功能,包括对β细胞增殖的控制、第一阶段胰岛素的分泌,以及机体低血糖时的胰高血糖素分泌……更为重要的是,这些细胞还控制着机体对糖的寻觅和饮食行为。
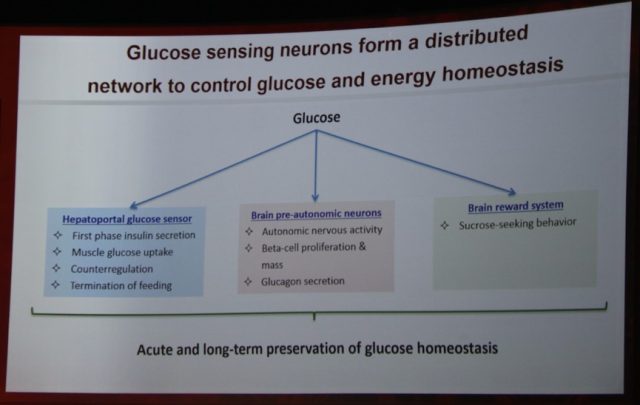
图 3 糖感神经元形成机体血糖和能量稳态的网络
最后,Thorens 教授总结道:「一系列的研究指出,在全身血糖感应细胞『网络』工作体系中,位于大脑中的「糖感神经元」起着重要作用,控制着全身的糖与能量代谢,这些细胞的失调将导致 2 型糖尿病的级联反应。」
Camillo Golgi 奖——与高血糖一样,复发性低血糖可直接导致糖尿病并发症
EASD Camillo Golgi 奖是以 1906 年诺贝尔奖获得者 Camillo Golgi 的名字命名的,主要奖励在糖尿病组织病理学、发病机理、预防和治疗并发症领域做出杰出贡献的学者。
今年授予了英国爱丁堡大学女王医学研究所 Brian Frier 教授。
Brian Frier 教授毕业于爱丁堡大学医学院,是爱丁堡大学女王医学研究所的糖尿病名誉教授,国际低血糖研究组成员,曾任爱丁堡皇家内科医师学院副院长。

图 4 Brian Frier 教授获奖现场
Brian Frier 教授的演讲题目为《复发性低血糖可致糖尿病的长期并发症》。
Frier 教授在演讲中说道,目前低血糖被认为是使用胰岛素和磺脲类药物治疗糖尿病时的一种不可避免的副作用。低血糖不能通过自我治疗来逆转,严重低血糖患者甚至可能导致患者昏迷、癫痫发作、心律失常、身体损伤。

图 5 低血糖阈值与机体症状
同时 Frier 教授强调,更不乐观的情况是,长期的反复发作的低血糖极有可能诱发患者发生——反调节激素缺乏症和低血糖意识障碍(IAH),从而导致患者认知能力下降,而 IAH 一旦确诊很难扭转,对患者生活质量和疾病控制将带来严重影响。
另外有证据表明,反复出现的低血糖可加速糖尿病患者大血管并发症的发生,并通过多种病理生理作用影响患者小血管的血流和功能,并且对于其中一些异常的功能,即使在患者血糖恢复正常后一周仍持续存在。
最后 Frier 教授总结道:「众所周知,血糖升高与血糖异常增加有着密切关系,血糖的升高可能导致局部血栓形成和炎症,并引发严重的心血管事件。但值得注意的是,复发性低血糖或许也是直接影响糖尿病并发症发生的重要机制之一,也就意味着糖尿病患者动态粥样硬化的恶化也可能是由于复发性低血糖与已知的巨细胞病变、微血管病变有关而导致。」
Albert Renold 奖——掌管β-细胞的 DNA 开关:「我被发现了」
Albert Renold 奖是为了纪念著名糖尿病学家 Albert Renold 教授而设立的,主要授予在胰岛研究领域做出杰出贡献的学者。
本年度的 Albert Renold 奖授予了英国伦敦帝国理工学院 Jorge Ferrer 教授。
Jorge Ferrer 教授是伦敦帝国理工学院遗传学系主任,NIHR 帝国生物医学研究中心的遗传与基因组学主题领导者。

图 6 Jorge Ferrer 教授获奖现场
Jorge Ferrer 教授的演讲题目为《DNA 开关,β细胞和糖尿病》。
Ferrer 教授在演讲之初谈及全世界有 3 亿糖尿病患者,而这个数字预计到 2030 年底将增至 5 亿人,糖尿病或将成为未来人们失明、截肢、肾脏疾病和过早死亡的主要原因,但是,人类仍缺乏对大多数糖尿病患者 DNA 中重要分子缺陷的了解。
目前,已知的基因组研究纳入了约 20,000 个基因,人类基因组中大量的 DNA 片段,它们充当着不同细胞中基因的开关。
Ferrer 教授所绘制的就是人类基因组中管理胰岛素分泌β细胞基因开关的 DNA 序列图,他的研究证明了:「 2 型糖尿病发生因素并不是基因变异所致,而是这些负责β细胞开关的 DNA 序列发生了改变而致使。」
该发现一定程度上证明,β细胞中基因的改变才是 2 型糖尿病发病机制的核心。
此外,Ferrer 教授还绘制了其他类型的基因组图谱,比如,有的图谱显示了开启胚胎胰腺基因表达开关的位置,证明导致儿童先天无胰腺这类罕见病的基因突变类型并不是由于基因断裂而致,而是由于胚胎胰腺开关基因的损坏导致。
Ferrer 教授这一系列研究突显了新型基因组技术对于解开糖尿病分子基础机制的作用,同时也揭示了:「从基因层面而言,影响糖尿病发生的不是基因的破坏,而是由于控制β细胞功能的基因『开关』发生了变化。」
会场现场,同样精彩

关注「丁香智汇」,关注EASD更多精彩