
在 2020 年 ACR 的痛风治疗指南中,别嘌醇被作为一线降尿酸药物推荐[1],但由于在黄种人中,别嘌醇因可引发致死性超敏反应,令不少医生对这一药物望而却步,甚至有医生表示:「不作第一个处方别嘌醇的医生」 但是,包括今年新发布的《痛风基层合理用药指南》[2]在内的多个国内指南也推荐别嘌醇为一线降尿酸药物。 作为一线推荐药物的别嘌醇,安全性到底如何,临床医生在应用别嘌醇时应该如何降低超敏反应的发生风险呢? 解答这个问题,需要先从别嘌醇的超敏反应综合征及其避免措施、适用人群这几个方面展开细说。
别嘌醇超敏反应综合征是什么?
大体上,药物不良反应分为 A 类和 B 类两种。
简单讲,可以把 A 类视为药物直接的毒性引起的各种不适;而 B 类反应称为超敏反应,由药物成分与机体免疫系统发生反应所产生的免疫损伤,表现多样。 A 类反应与药物的剂量呈明确的相关性,而 B 类反应与药物剂量的关系相对不够紧密,主要与自身免疫状态相关。 别嘌醇令人担心的,就是可能引发较为严重的超敏反应——别嘌醇超敏反应综合征(AHS)。 AHS 还有一些其他的名称,如别嘌醇相关严重皮肤不良反应(SCAR),在表现上与药物诱发超敏反应综合征(DiHS,又称 DESS)或 Stevens-Johnson 综合征(SJS)和中毒性表皮坏死溶解症(TEN)有时存在重叠,具体情形如下图: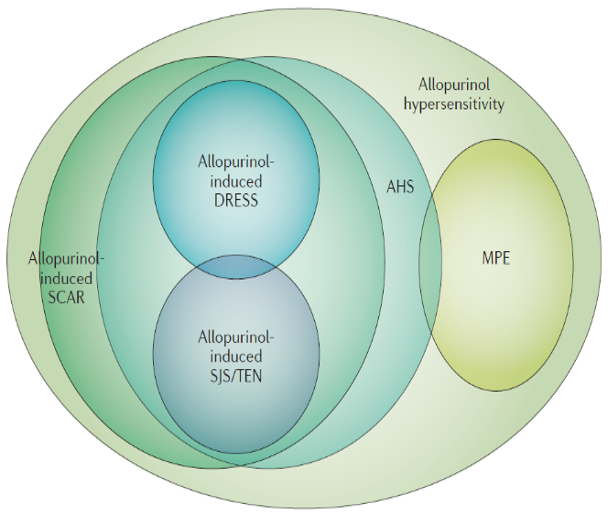
注:别嘌醇相关超敏反应的表现,AHS:别嘌醇超敏反应综合征,DRESS:药物诱发超敏反应伴嗜酸细胞增多综合征,MPE:斑丘疹样皮疹,SCAR:严重皮肤不练反应,SJS/TEN:Stevens-Johnson综合征和中毒性表皮坏死溶解症[3]
症状:
当发生 AHS 时,可能出现多形红斑、表皮溶解、剥脱性皮炎、斑丘疹等多样性皮疹,常伴有发热、白细胞增多、嗜酸细胞增多以及肝肾功能异常。 AHS 在不同地区的发生率不等,我国台湾的一项调查表明,在新起始治疗的人群中 AHS 的发生率大约为 0.5 例/百患者/年[4]。虽然 AHS 并不常见,但同一研究的数据显示 AHS 发生后的致死率为 8.3% [4],其他报道中的死亡率为 9%~20%[5],的确需要引起重视。 诊断:
依据 2005 年 Gutierrez-Macias A 等制订的 AHS 诊断标准[6] 注:AHS 的诊断标准
注:AHS 的诊断标准
治疗:
目前对于 AHS,除了停药+支持治疗,并无其他有效治疗方法。
AHS 相关危险因素:
AHS 属于 IV 型超敏反应,目前认为是由于别嘌醇的活性代谢产物氧嘌呤醇与 HLA 分子结合进而导致 T 细胞活化所引起的免疫反应。当存在 HLA-B*5801 基因型时,这种反应发生率显著增加。
此外,相对高的药物浓度也与 AHS 相关,肾功能不全、合并应用利尿剂都会增加氧嘌呤醇的浓度。
与 AHS 相关的危险因素可以分为可干预性与非可干预性两类: 注:与 AHS 相关的危险因素 有研究显示,AHS 的中位发生时间为起始治疗后的 30 天,90% 的案例在治疗后 180 天内发生(下图)[7]。
注:与 AHS 相关的危险因素 有研究显示,AHS 的中位发生时间为起始治疗后的 30 天,90% 的案例在治疗后 180 天内发生(下图)[7]。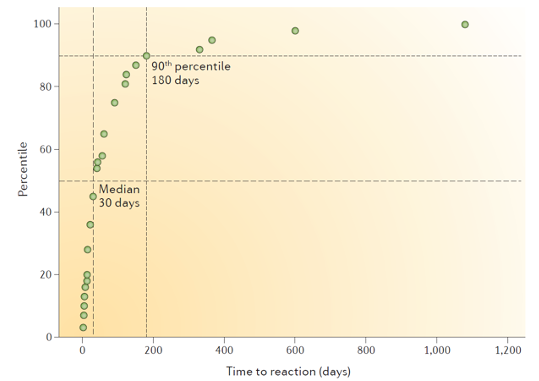
注:AHS 的发生时间,中位时间为 30 天,90% 于用药后 180 天发生。

如何避免 AHS 的发生?
主要的措施包括:
用药前筛查 HLA-B*5801 基因
从小剂量开始给药
避免联合应用利尿剂
对于肾功能不全的患者慎重用药
密切关注用药后的反应
HLA-B*5801 阳性的个体应用别嘌醇需要慎重,但并非不能应用。 有研究发现, HLA-B*5801 阳性群体中,肾功能正常者 AHS 发生率不超过 2.7%[8],而肾功能不全者中的发生率高达 18%[9]。因此,对于肾功能不全的个体,应用别嘌醇要慎重。 ACR 指南推荐,起始治疗时,别嘌醇的日剂量不应超过 100 mg[1],对于肾功能不全者,剂量应进一步调低,有研究发现,每日别嘌醇剂量不超过 1.5xGFR(mg)时,可以减少 AHS 的发生率[7]。 鉴于发生 AHS 的中位时间为 30 天,在起始治疗的第一个月,尤其应该关注有无皮疹等表现;此外,即使起始治疗的前几个月没有发生 AHS,也不能完全对AHS 放松警惕。
哪些人群适用别嘌醇?
肾功能正常且 HLA-B*5801 阴性的个体,应用别嘌醇相对安全。
对于 HLA-B*5801 阳性的个体,如果肾功能正常,发生 AHS 的风险高于阴性个体,但仍可尝试从小剂量起始治疗,如果肾功能不全,应尽可能避免应用别嘌醇。 目前一些医疗机构无法进行 HLA-B*5801 检测,针对这种情况,也可应用别嘌醇,但剂量应该从更低水平开始,每日 50 mg 甚至隔日 50 mg,四周后如无不良反应发生,可根据尿酸下降情况调整用量。
为何别嘌醇是首选药物?
目前的多个指南均推荐抑制尿酸生成的药物作为一线降尿酸药物,这类药物包括了别嘌醇及非布司他,而非布司他因心血管安全性存在可能的风险,不被作为首选药物。 (图自:用药助手 App)
(图自:用药助手 App)
别嘌醇的 AHS 风险在黄种人中虽然较欧美偏高,但通过对 AHS 的危险因素进行了解,并合理选择适用人群,在密切监测药物反应的前提下,别嘌醇还是可以作为降尿酸的首选药物。

限时 7 天免费读

策划 | 圆脸大侠
题图 | 站酷海洛投稿 | drugs@dxy.cn参考文献:
[1] FitzGerald JD, Dalbeth N, Mikuls T, et al. 2020 American College of Rheumatology Guideline for the Management of Gout[J]. Arthritis Rheumatol, 2020. doi: 10.1002/art.41247
[2]痛风基层合理用药指南[J]. 中华全科医师杂志, 2021, 20(6): 631-638. doi: 10.3760/cma.j.cn114798-20210317-002
[3]Stamp LK, Day RO, Yun J. Allopurinol hypersensitivity: investigating the cause and minimizing the risk[J]. Nature reviews. Rheumatology, 2016, 12(4): 235-242. doi: 10.1038/nrrheum.2015.132
[4]Yang C-Y, Chen C-H, Deng S-T, et al. Allopurinol Use and Risk of Fatal Hypersensitivity Reactions: A Nationwide Population-Based Study in Taiwan[J]. JAMA internal medicine, 2015, 175(9): 1550-1557. doi: 10.1001/jamainternmed.2015.3536
[5]Ramasamy SN, Korb-Wells CS, Kannangara DR, et al. Allopurinol hypersensitivity: a systematic review of all published cases, 1950-2012[J]. Drug Saf, 2013, 36(10): 953-980. doi: 10.1007/s40264-013-0084-0
[6]Gutierrez-Macias A, Lizarralde-Palacios E, Martinez-Odriozola P, et al. Fatal allopurinol hypersensitivity syndrome after treatment of asymptomatic hyperuricaemia[J]. BMJ, 2005, 331(7517): 623-624. doi: 10.1136/bmj.331.7517.623
[7]Stamp LK, Taylor WJ, Jones PB, et al. Starting dose is a risk factor for allopurinol hypersensitivity syndrome: a proposed safe starting dose of allopurinol[J]. Arthritis and rheumatism, 2012, 64(8): 2529-2536. doi: 10.1002/art.34488
[8]Hung S-I, Chung W-H, Liou L-B, et al. HLA-B*5801 allele as a genetic marker for severe cutaneous adverse reactions caused by allopurinol[J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(11): 4134-4139. doi:
[9]Jung J-W, Song W-J, Kim Y-S, et al. HLA-B58 can help the clinical decision on starting allopurinol in patients with chronic renal insufficiency[J]. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association - European Renal Association, 2011, 26(11): 3567-3572. doi: 10.1093/ndt/gfr060
