由中日友好医院李平教授和解放军总医院谢院生教授主编的《糖尿病肾病——中西医结合诊疗与研究》一书将于近日出版,该书分为上、中、下三篇,全面介绍了糖尿病肾病的流行病学、诊断及鉴别诊断、中西医治疗及进展等内容,力求「源于中医,高于中医,源于西医,高于西医」。本人参与了其中「糖尿病肾病早期诊断和病情评估生物标志物」部分的编写,现呈现给大家评阅。
(第一部分请参阅《糖尿病肾病早期诊断和病情评估生物标志物(一)》)
第二部分 新型标志物
其他潜在的 DKD 风险和进展信号在成为可靠的疾病标志物前,还需要进一步证据支持。候选的标志物包括尿液蛋白绑定的晚期糖基化终末产物(AGEs)、特定的氧化应激标志物和纤维化细胞因子,例如结缔组织生长因子(CTGF)、转化生长因子β(TGF-β)、胱抑素 C 和脂肪酸结合蛋白家族中的肾小管标志物。新增的标志物包括成纤维细胞生长因子 23(FGF-23),尿液 IV 型胶原蛋白以及循环或尿液微小核糖核酸(microRNA)。
(一)炎症标志物
慢性微炎症状态在 DN 的发病过程中起重要作用,某些关键炎症因子为 DN 的病情判断提供了关键线索。
通过第一次乔斯林肾脏研究(即 1 型糖尿病患者微量白蛋白尿自然病程研究)中 145 例患者的尿标本检测,发现白介素 6(IL-6)、白介素 8(IL-8)、单核细胞趋化蛋白 1(MCP-1)、干扰素γ诱导蛋白(IP-10)、巨噬细胞炎性蛋白 1δ(MIP-1δ)的尿浓度在肾功能下降的患者中显著升高,且出现早期肾功能下降(每年 GFR 下降>3 mL/min/1.73m2)者这 5 种炎症标志物的基线水平高于肾功能稳定者,两种以上炎症标志物浓度升高的患者出现早期肾功能下降的风险增加 5 倍。
第二次乔斯林肾脏研究的横断面分析发现,炎症相关标志物-可溶性肿瘤坏死因子受体 1 和 2(sTNFR1, 2)与 cC-GRF 水平呈显著负相关。
系列的临床研究进一步阐明了 TNFRs 对 1 型和 2 型糖尿病患者肾脏病情转归的预测价值。Gohda 等的研究证实血浆 TNFR 水平对 1 型糖尿病患者的预后有提示意义,该研究纳入了两次乔斯林肾脏研究中 cC-GFR 正常的 628 例患者,TNFR2 水平处于最高四分位距的患者 12 年后达到 CKD-3 期的累积发生率为 60%,而其他四分位距的患者仅为 5%-19%。Cox 比例风险模型分析显示,TNFR2 水平处于最高四分位距的患者发生早期肾功能下降的风险比其他患者高 3 倍 (HR = 3.0)。
基于 DCCT/EDIC 研究(糖尿病控制与并发症研究/糖尿病干预及并发症流行病学研究)数据的结论同样证实,炎症标志物-sTNFR1、2 和 E 选择素的升高是 1 型糖尿病患者显性蛋白尿进展重要的独立预测因子。Pavkov 等的最新研究显示 TNFR1、2 对 2 型糖尿病患者的 ESRD 也具有良好的预测价值。
Niewczas 等通过 410 例 2 型糖尿病患者的观察性研究提出 TNFR1 的基线水平能够独立预测 12 年后 ESRD 的进程,这种关联性在尿蛋白正常的患者中更强,提示血浆 TNFR 有望成为比蛋白尿更有效力的 ESRD 预测标志物。
(二)氧化应激标志物
线粒体 ROS 产物 8-羟基-2』-脱氧鸟苷 (8-OHdG) 是高糖诱导肾脏损伤的关键调节因子,也是评估人体氧化应激状况的有效手段。研究显示,尿 8-OHdG 的升高与 2 型糖尿病 DN 患者的蛋白尿进展相关,多因素 logistic 回归分析提示它在多种危险因素中表现出较好的预测价值。然而,也有研究认为尿 8-OHdG 水平对 DN 进展的预测能力无法超越 ACR。
核因子(NF)-E2 相关因子 (Nrf2) 是调节细胞内抗氧化的主要转移因子,被证实可能有肾脏保护作用,它的调节物-甲基巴多索隆被认为是治疗 DN 有前景的新药,并开展了大型临床试验。然而,虽然实验室和临床研究均证实甲基巴多索隆能够逆转 DN 的 GFR,但因其增加心衰风险的副作用而被终止于Ⅲ期临床试验。
(三)细胞因子
尿结缔组织生长因子(CTGF)水平与 ACR 水平密切相关,微量白蛋白尿患者的 CTGF 比尿蛋白正常的患者高 10 倍,显性蛋白尿患者可高出 100 倍。尿 CTGF 的排泄和 1 型糖尿病肾病患者的蛋白尿、GFR 进展相关,血浆 CTGF 基线水平是显性蛋白尿患者 ESRD 和死亡的独立危险因素。
成纤维细胞生长因子 23(FGF-23)是磷酸代谢的重要调节因子。一项 2 型糖尿病合并显性蛋白尿患者的研究通过 33 个月的随访发现,血清 FGF-23 水平是肌酐翻倍、透析、死亡等硬终点的独立预测因子。
足细胞 B7-1 的可溶性配体 CD28(sCD28)升高预示着 DN 进展至 ESRD 的高风险。进展至 ESRD 患者的血 sCD28 基线水平高于肾功能稳定的患者。通过调整年龄、eGFR、糖化血红蛋白、尿蛋白等协变量,多因素分析表明 sCD28 是 DN 进展至 ESRD 的独立危险因素。
(四)新型肾小管损伤标志物
早在 10 年前就发现,除肾小球损伤外,肾小管间质损害也是 DN 进展的重要危险因素。最新的病理研究证实肾小管间质损害能够预测 2 型糖尿病肾病患者的快速肾功能下降(每年 GFR 下降>14.9%)。
反映肾小管功能障碍的脂肪酸结合蛋白 (fatty acid-binding protein, FABP) 是 DN 预后标志物研究的新热点。FABP 家族的重要成员肝型脂肪酸结合蛋白 (liver-typeFABP,L-FABP) 为内源性抗氧化剂,分布在人近端肾小管的胞浆内,很少在啮齿动物的肾脏表达。
多中心试验表明,尿 L-FABP 在预测 CKD 进展方面比蛋白尿更敏感,对 DN、AKI 的早期诊断和病情判断也更为有效,被日本卫生部批准为新的能够应用于临床的肾小管损伤标志物。它在尿液中的浓度与 DN 患者蛋白尿、ESRD 的进展速度相关。对 eGFR >60 mL/min/1.73m2的 104 例 2 型糖尿病患者随访 4 年,研究结果显示高浓度 L-FABP 是 DN 病情进展有力的独立预测因子。
一项 2 型糖尿病患者的横断面研究发现,心脂肪酸结合蛋白 (heart FABP, H-FABP) 是唯一与 eGFR 相关的肾小管标志物。尿 L-FABP 同样可以独立预测 1 型糖尿病患者微量白蛋白尿的进展。
肾脏损伤分子 1(kidney injury molecule-1, KIM-1)、中性粒细胞明胶酶相关脂质运载蛋白 (neutrophil gelatinase associated lipocalin,NGAL) 也是著名的近端小管损伤标志物。研究显示,合并蛋白尿的 1 型糖尿病患者尿基线 KIM-1 和 NGAL 水平越高,GFR 下降越快。但当考虑了蛋白尿、糖尿病病史、血糖和血压控制水平等 DN 的传统危险因素后,这种关联就不再具有统计学意义。
另一项研究对尿蛋白正常且 eGFR ≥ 60 mL/min/1.73m2的 2 型糖尿病患者随访 4 年,发现尿 KIM-1、非转移性黑色素瘤糖蛋白 B(glycoprotein nonmetastatic melanoma B, Gpnmb) 与患者 eGFR 的年下降率相关。同样的,当调整了基线尿蛋白水平、糖化血红蛋白等已知危险因素后,这种关联的统计学意义也消失了。然而,也有一些前瞻性研究发现 NGAL、KIM-1、Gpnmb 和 2 型糖尿病患者的蛋白尿变化没有相关性。
(五)微小 RNA
基础研究发现 miRNAs 可以作为 DN 进展的标志物,研究热点主要集中在 TGFβ调节的 miRNAs,如 miR-21、miR-29 家族、miR-200,以及 miR192。然而,将 miRNAs 作为 DN 病情判断标志物还存在以下问题:多停留在 DN 患者体液 miRNAs 轮廓的描述上;对于尿标本的检测只做了 miRNAs 的定量而未明确它们的细胞来源;缺乏 miRNAs 表达和 CKD 临床表现相关联的原始数据。
Zampetaki 等较早在大型 2 型糖尿病患者队列中评价了血浆 miRNAs 的预后意义,发现 miRNA 能鉴别出 70% 进展性的糖尿病患者,这一预测价值高于现有临床指标。56 例行肾活检明确病理诊断的 CKD 患者尿沉渣 miRNA 检测显示,其中 17 例 DN 患者表现出特异性的 miR-15 降低,随访发现 miR-15 与基线尿蛋白水平和 GFR 降低速度呈负相关。
匹兹堡糖尿病流行病学(Pittsburgh Epidemiology of Diabetes Complications,EDC)研究中,在 40 例 1 型糖尿病患者的尿标本 miRNAs 检测发现 miR-429 等 27 种差异 miRNAs,主要集中于 DN 相关的生长因子信号通路和肾纤维化信号通路,对 DN 的早期诊断、病程监测、病情判断等有重要意义。
(六)蛋白质组学发现的新型标志物
尿蛋白质组技术为尿蛋白的鉴别和定量提供了系列方法,也发现了一些用于 DN 病情判断的新型尿标志物,如 CKD273,正常白蛋白尿伴 CKD273 阳性的患者出现显性白蛋白尿的风险显著增加,并能先于微量白蛋白尿而预测。CKD273 阳性分类模式有助于鉴别有 DN 进展风险的正常蛋白尿患者,其预后意义优于 DN 的其他传统危险因素。
早期肾功能下降的患者相对肾功能稳定的患者,α-1(Ⅳ) 胶原、α-1(V) 胶原和细胞粘合素蛋白 X3 种尿蛋白的片段水平下降,而肌醇戊基磷酸 2 激酶、闭合小环蛋白 3 和 FAT 抑癌基因 2 这三种蛋白的片段水平上升,为预测合并微量白蛋白尿的 1 型糖尿病患者早期肾功能下降风险提供了可能。
(七)遗传标志物
遗传和表观遗传因子可以影响 DKD 的发生和发展。尽管有证据表明 DKD 发展的基因易感性,但是很难确定致病基因。DKD 的家族聚集性是一个公认的现象。伴有糖尿病的患者比没有糖尿病家族史的患者 ESRD 风险高 5 倍。与 DKD 发生易感性相关的候选基因见下,在这些候选基因中,与 RAAS 相关的基因研究最为广泛。
潜在的 DKD 风险生物标志物需要进一步研究,风险预测还应该继续关注家族史、吸烟史、绝对的白蛋白排泄率、精确的 GFR 测量、血糖控制、血压测量和血浆脂质水平。糖尿病患者发展产生 DKD,GFR 降低到发展成为 ESRD,依然很难确定。由于没有 DKD 诊断和进展的金标准,对于 DKD 相关标志物的探索很困难。DKD 早期风险标志物的探索是临床实践和临床试验的需求。
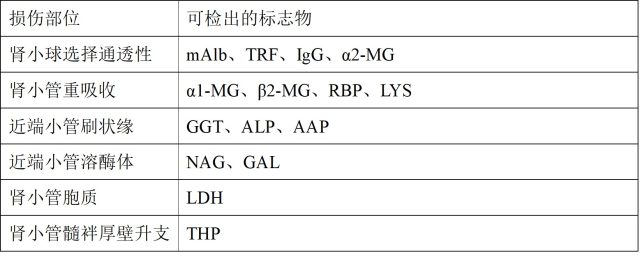
(八)标志物的联合应用:标志物的联合分析,提高了对 DKD 早期损伤检出的阳性率,使得对 DKD 患病者的诊治更加全面合理(表 1)。
表 1 肾损伤标志物的意义
编者简介:李江,毕业于中南大学湘雅医学院,现就职于中日友好医院检验科,副主任技师,主要从事临床生化与免疫学检验的方法学及临床应用、慢性病监测与管理、临床检验质量控制等工作。
