这片土地上关于中医的若干最新状况,告诉我们一个事实:中医最好的时代已经到来。
11月的最后一天,NATURE 官网上发表了一篇文章,对即将来临的中医的黄金时代作了些点评:
从 2018 年初起,在中国,传统中药将不再需要通过人体安全性和有效性临床试验。药企只要拿得出『(古代)经典名方』作为依据,那两项成本高昂、周期漫长的临床试验就可以靠边站了,不再是阻碍;
只需要提供临床试验之前基于动物或体细胞的药理与药物毒性研究即可;
这份古代经典名方清单将由国家中医药管理局和中国食品药品监督管理局共同拟定。
根据今年 7 月颁布的中医药法,中医药专业毕业后可以跳开国家现代医学考试,只要以古来传统的学徒形式通过技能测试就可以从业;中医诊所的开设也不需要主管部门审核,像开发网站那样备个案就可以了——这一次的冲击已经足够给力,它意味着中医的机构与从业人员的准入门槛的降低,也抛弃了现代医学所设立的基本原则。
一个是对于从业方的解绑,一个是对于医药品的解绑。

当现代医学缺席之后,原有的挑战和质疑的逻辑已不复存在,就好比你打算和人在一个擂台上打拳击的时候,忽然有人把你脚下的地板全部抽空,你直接坠到楼下,和对手都已经不在一个空间维度上,于是永远不会再有交手的可能以及必要了。
在现代医学里为什么临床试验必不可少?这个话题可以讲一千零一夜,这里有几个例子:
众所周知,激素替代疗法(HRT)能够很好地改善更年期以及绝经之后女性的诸多不适,改善生活品质。
但推广时间久了、应用普及了之后,很多机构与医生开始将HRT应用到其他领域,譬如心脏病的预防。
他们凭借自己的从业经验,认为 HRT 或对心脏病预防有益。在现代医学的用药或治疗手段上、这就属于标签外应用、也就是说此时某种疗法的治疗目的已经在其原初所界定的范围之外了。
这种情况可能产生什么影响呢?可能有效、可能无效、可能有效但同时有害、可能无效同时却有害。
既然出现了这样新的应用趋势,医学就需要对其进行严谨的研究。因为这不是闹着玩的。假如运气好有效、或者运气一般无效倒也罢了,但万一运气不好,有效但同时有害并且害处超过了效果,甚至下下签地无效却同时有害的话,那可是人命关天的事情。
因此美国国家心肺血液研究所开始调查 HRT 是否真的有利于绝经后女性的心脏病预防,以及考察会不会有什么潜在的风险。
结果发现:
HRT 运用前几年中、女性心脏病风险不降反升;
HRT 会升高中风与血栓的风险;
雌激素与孕激素联用者、乳腺癌风险上升。
这是科学洞察的结果。
基于此,今日的美国 FDA 对于 HRT 的应用界定比早先更加严格:
HRT 绝不可用于心脏病预防;
HRT 可用于改善更年期以及绝境后症状,必须充分衡量对比收益与(癌症诱发等)风险;
HRT 可用于改善更年期以及绝经后症状,必须坚持显效内最低剂量以及最短疗程之原则、绝对不能为了效果显著怎么爽怎么用。
现代医学里,直觉是不可靠的。
再牛逼的医生,仅凭自己的感觉和经验完全可能出错。专科医生一辈子能够看的病人人数比起动辄数十万人的研究相差甚远,当中存在的认知偏差、安慰剂效应以及其他混淆因素更是毋庸赘言。
到底是不是真的有效,不通过科学的话谁都说不清楚,无论是患者还是医生。
现代医学里,某种药物和疗法的潜在风险,不是任何时候都能简单说清楚的。
很多急性不良反应与中毒反应还可能通过经验来总结,譬如你不小心服用了含草乌头的中药材,几小时之后嘴唇发麻视线模糊。
然而一旦这种不良反应中毒反应是慢性的,就需要很多年乃至数十年才能显示『威力』,尤其是和癌症诱发相关的时候,靠传统经验和观察哪怕数千年都不可能得出结论、甚至根本都联想不到一起。马兜铃酸类中草药材就是一个最好的证明。
这是因为有太多混淆因素葛藤纠缠在一起、就像我们幼儿园时代都画过的小花猫钓鱼图一样:小花猫咪手里的钓鱼线乱麻一样结成一团、最后末端是许许多多的鱼、中间九曲十八弯、各种拐点和转向、没有适应过科学思维的人根本理不清头绪、不可能理得清头绪。
更可怕的是,诱发癌症的责任问题比小花猫到底钓了什么鱼更加复杂:
就算常年吃马兜铃酸类中草药的患者得了尿路上皮癌或者肾癌、他都没法去申诉赔偿,这是因为你根本没法证明你的癌是以马兜铃酸类草药为主导引发的——日常生活中各种致癌物质、致癌环境、致癌生活方式实在太多了,每一种角色都在对癌症的形成捅刀子,但目前的科学常常无法确切锁定每一个个例中,到底哪一个癌症风险捅了你几刀,究竟是从犯还是主犯。
所以,在慢性风险尤其癌症上,出了事情对不起,所有问题请你自己扛。人类能做到的最佳善待自己的方式,就是从一开始就不要让捅刀子的歹徒有机会靠近。
怎么才能知道是不是歹徒?靠科研,靠临床试验。临床试验理应是药物批准道路上必不可少的约束条件,因为临床试验是针对人进行的,你生病的时候服药的不是你家猫狗,是你本人。这一个环节是不可以跳跃的。
这里有一个的故事,发生在 60 年前:
有一款西药:Thalidomide——商品名『反应停』。
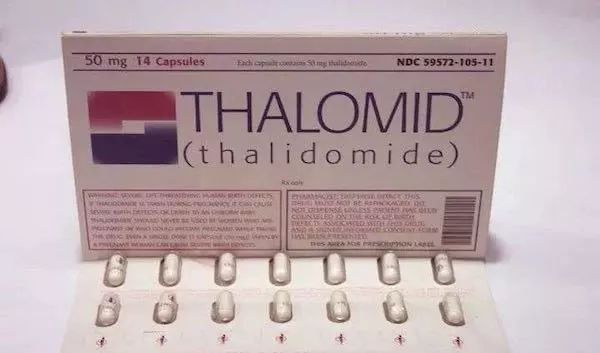
这种中枢神经抑制剂有着非常良好的镇静催眠,极其有效的妊娠反应抑制作用,由当时西德药厂 Chemie Grünenthal 研发完成,1957 年在欧洲上市,人气爆棚,席卷欧洲、日本、澳洲还有拉美。
大伙儿都惊呆了:这款药物是如此好用,几乎没有表现出任何副作用。孕妇最痛苦的那几个月里难道还可能有更好的药物伴侣吗?
然而这么『好』的东西却竟然没有能够进入美国,不是因为不想进去,而是美国 FDA 对这款药物实施了极其冗长繁琐严苛的调查研究。
有好几位官员表达了顾虑:该药动物实验结果和人体实验结果差距很大(对照前文提到的 2018 年新规则第二要点:只需要提供临床试验之前基于动物或体细胞的药理与药物毒性研究即可),由此怀疑动物实验所获毒理学数据的可靠性。
其中最重要的人物就是 FDA 的一位女性药理学家:Frances Oldham Kelsey。

她顶住了来自药厂和其他方面的压力,反反复复反反复复强调一句话:『还要研究、还要研究、还要研究』。
药厂要求药物获得上市批准的申请提出了多达六次,结果每一次都被无情拒绝。
就这样拖拖拉拉到最后,这款药物最终没有能够撬开美国的大门。
然而后来的事实证明,这简直是美国人民,尤其是美国准妈妈们的大幸——1960 年代初开始,欧洲和日本相继发现新生儿畸形比例异常飙升。
相继而至的流行病学研究锁定了反应停和新生儿畸形之间的相关性。
医学界开始严格调查反应停,发现反应停对于灵长类动物有强烈致畸性。1961 年秋天 Chemie Grünenthal 公司撤回西德市场上所有反应停,立即其他国家都跟进,但已经晚了——因反应停而先天畸形的新生儿人数超过一万,还有无数因反应停导致的本可避免的流产案例。此事在日本引发巨大社会反响,甚至一度对西药产生恐慌。
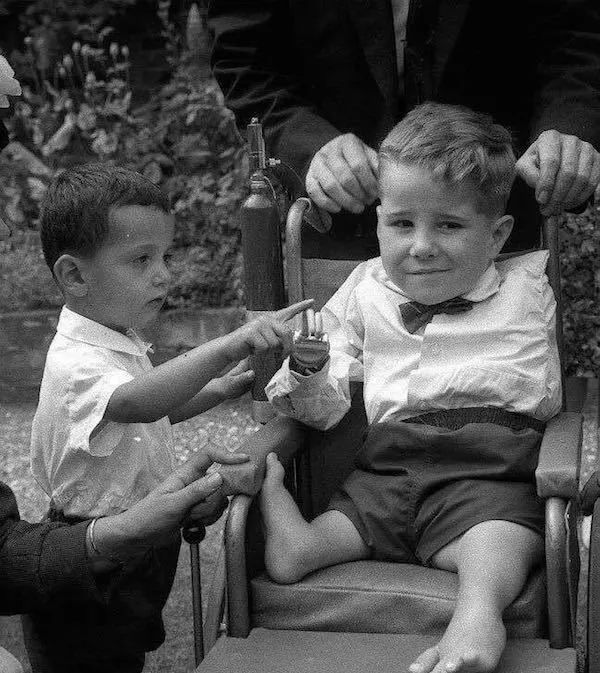
反应停:人体毒理没有洞察透彻的代价
Frances Oldham Kelsey 因此成为很多人眼中的英雄,1962 年获得肯尼迪总统授予的『杰出联邦公民服务总统奖』,2010 年 9 月美国FDA再度授予她以她的姓命名的 Kelsey 奖。

总统对她表示感谢
老太太身体非常好,一直活到 2015 年 8 月,享年 101 岁。
即便严格依照美国 FDA 流程,旷日持久成本高昂地完成包括临床试验在内的所有三期临床考察,都不能 100% 确保药物上市之后完全没有问题,所以 FDA 才设置了第四期,也就是上市后观察期。
哪怕 FDA 的四期临床试验都无法完全压住潘多拉魔盒,总有一丝缝隙里飞出意想不到的幺蛾子——直接跳开临床试验的话会出现什么后果,我不敢妄自揣测。
然而在这片土地上,临床试验这一至关重要的步骤从明年年初开始,就要对中药网开一面了。
如同脚下的地板被突然掏空,坠落下去,事情和事情之间无法再基于现代医学思维擂台去切磋、讨论与比较。
从此变成了一种滑稽的双盲:不是现代医学有效性试金石的随机双盲对照试验,而是现代医学从此对传统医学盲,传统医学对现代医学盲,互相割裂,互相越行越远。
